氧化电势和还原电势的是什么?区别
2023-10-24 07:46:20 作者:小米儿Sunny 文章来源:66软件下载 阅读次数:271
在一般应用中,氧化还原电位和电极电势两个名词混用。
氧化还原电位越负,越倾向于发生氧化反应;氧化还原电位越正,越倾向于发生还原反应。标准电极电势的数值越大,它的氧化态的氧化性越强,还原态的还原性越弱;标准电极电势的数值越小,它的氧化态的氧化性越弱,还原态的还原性越强。电势,根据百度解释就是电能量的趋向!电势也是电位,在电路中某一点这种趋势的大小!这点前提是选取零点电位,因为要有一个点作为标准,为什么选取的非得是零点电位。因为大多数人最熟悉的是正数!所以一般都会把最低点电势作为零点电位。
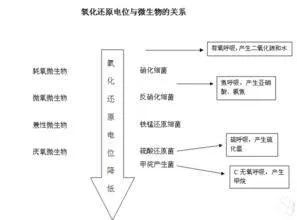
氧化电位”这个词不大常见。“标准氧化电位”这个词更少见。
标准电极电势都是英文语境下的“还原电势”,也就是氧化态被还原为还原态的电位。电极的组成一般写为“氧化态/还原态”,表明是氧化态被还原为还原态的电位。
仔细考察起来,标准XX电位都是一种平衡电位。如果组成电解池(或者说,电极电势由外电路来维持),在这个电位下,还原态和氧化态的活度之比为一,没有“净”氧化或者还原反应产生。所以干脆可以称之为氧化还原电位(redox potential)。只要指明氧化态和还原态,就不会产生误解。


 速通大赛2025:善款255万美元创新纪录
速通大赛2025:善款255万美元创新纪录 奥特曼闯关游戏推荐合集
奥特曼闯关游戏推荐合集 巫师3团队与其他工作室合作设计新任务
巫师3团队与其他工作室合作设计新任务 心态崩了看片这么多年女主角是谁【图片来源】
心态崩了看片这么多年女主角是谁【图片来源】 赵露思球操高清图片【附视频】
赵露思球操高清图片【附视频】 Zlata柔术cosplay玛丽莲梦露
Zlata柔术cosplay玛丽莲梦露 金融考试准题库
金融考试准题库 多看点
多看点 眉山日报
眉山日报 小嘀咕
小嘀咕 潇洒桐庐
潇洒桐庐 壹家购
壹家购 天下医生医生版
天下医生医生版 小羞漫画壁纸
小羞漫画壁纸 优到客店员
优到客店员 家庭流水账
家庭流水账